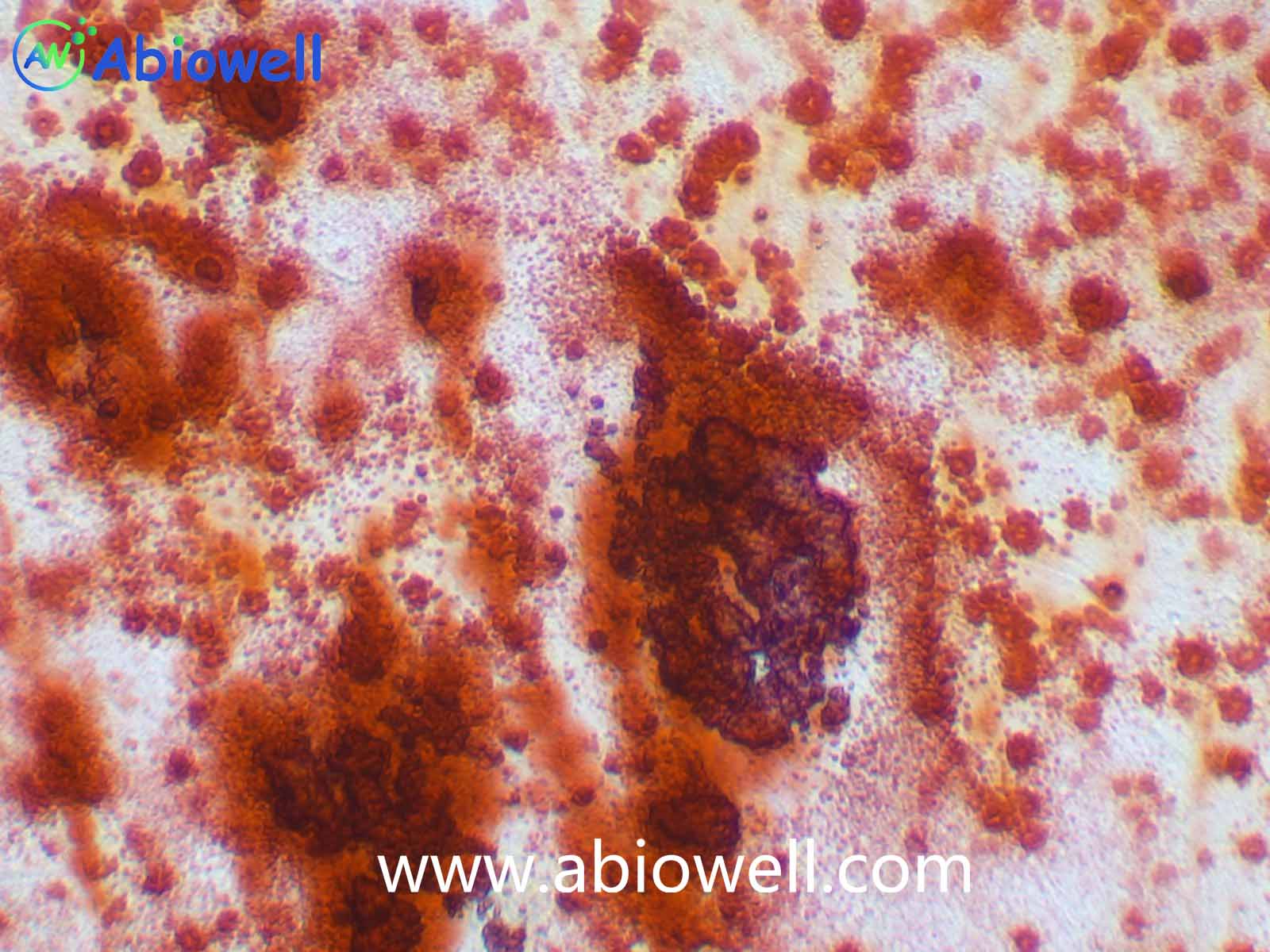
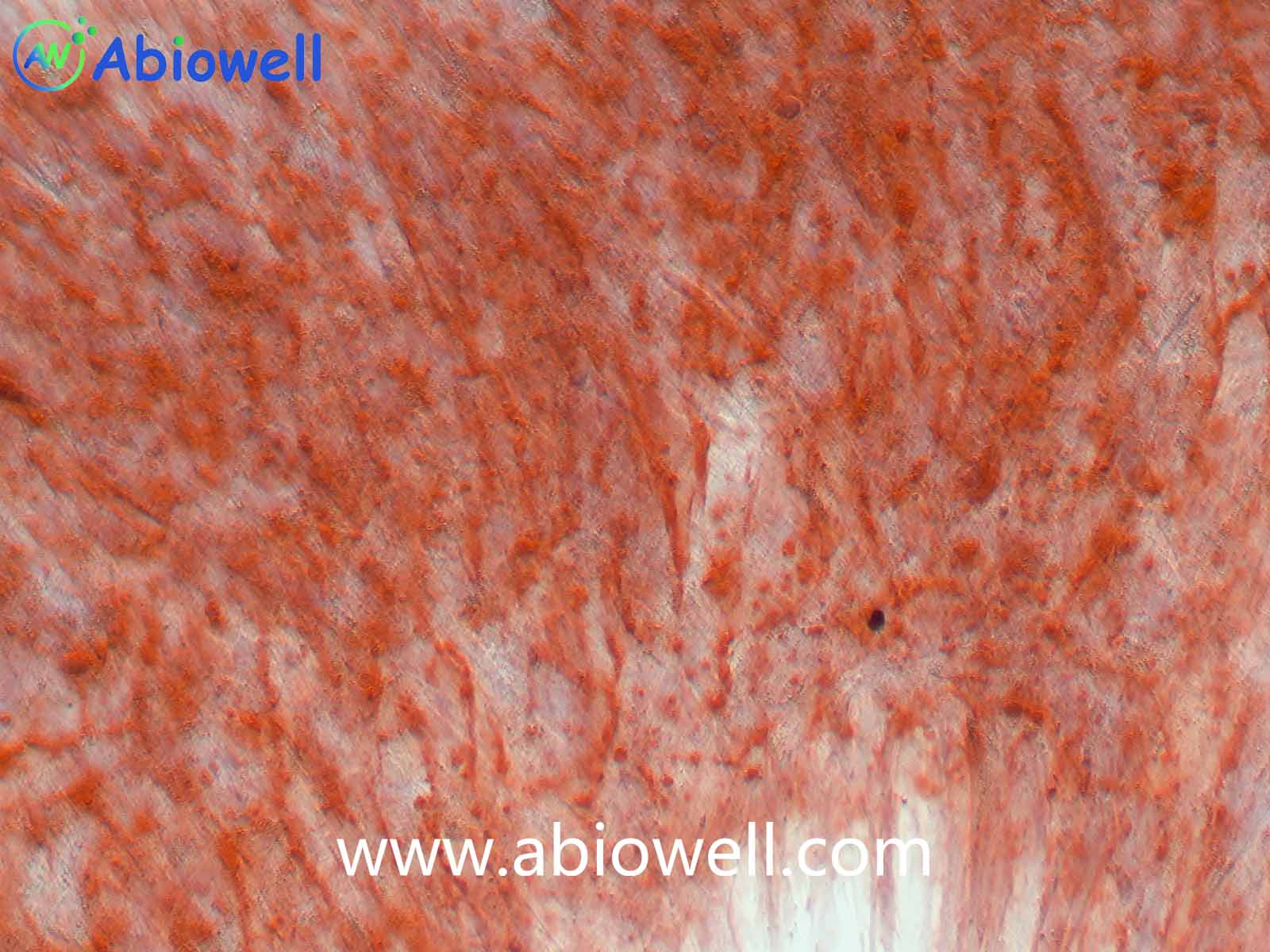
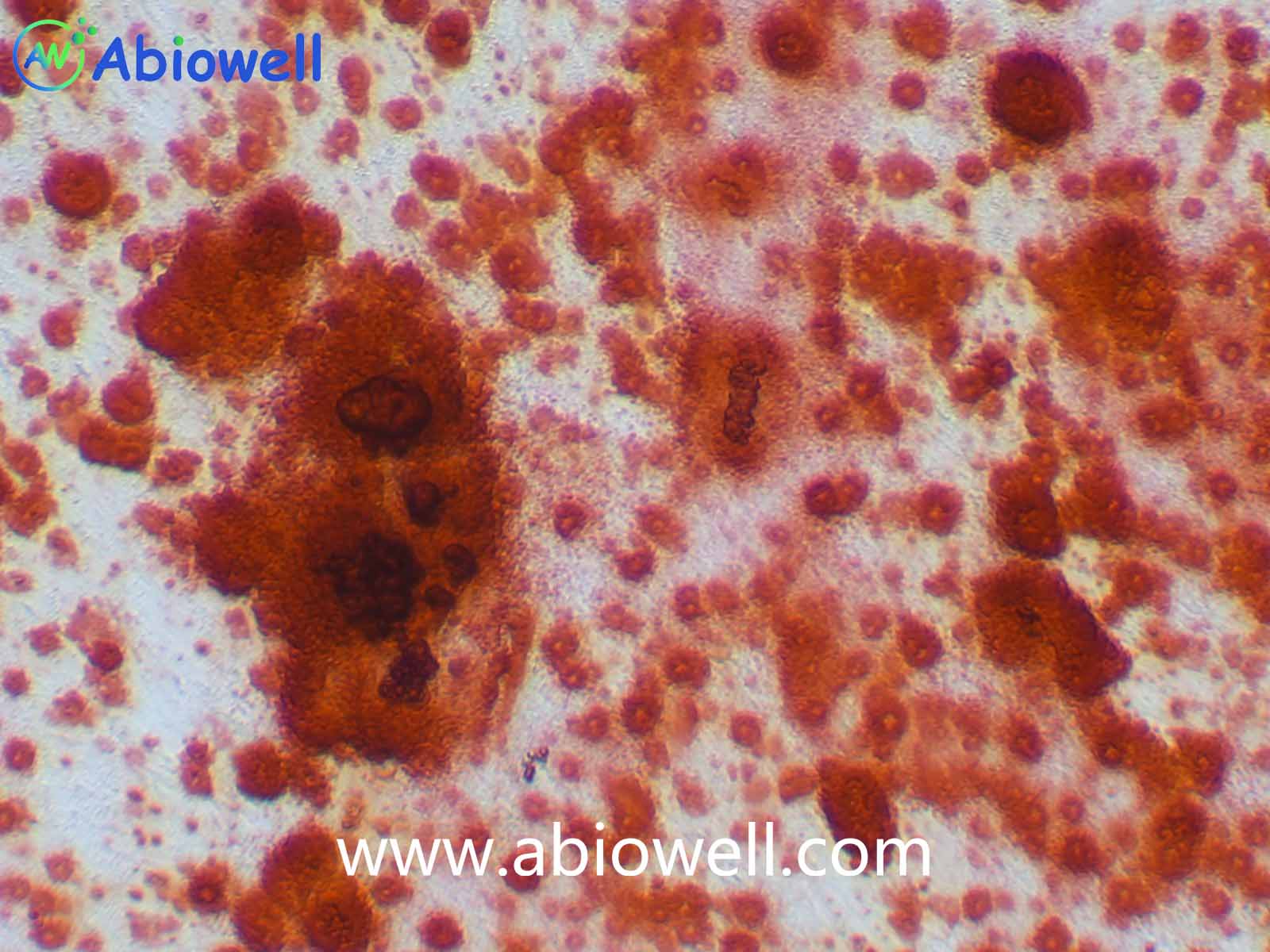
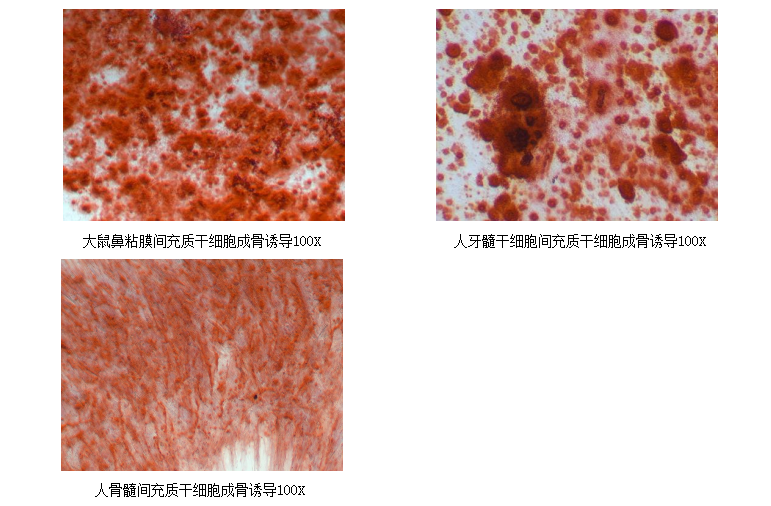
成骨诱导分化培养基
一、产品介绍
本产品专门为干细胞成骨诱导分化而开发,针对不同类型的间充质干细胞的特性优化分化试剂的配方。本产品经过实验测试,可以用于不同类型间充质干细胞的成骨诱导。
本产品含血清成分,仅用于科研用途,不可用于诊断、治疗、临床及其他用途。
二、产品规格
名称 | 货号 | 规格 |
细胞成骨诱导分化培养基 | AW-MY001a | 100mL |
细胞成骨诱导分化培养基 | AW-MY001b | 200 mL |
三、 产品组成成分及保存条件
成分 | 体积(100ml/200ml) | 保存条件 | 有效期 |
细胞基础培养基 | 89ml/177ml | 2-8℃ | 1年 |
特级胎牛血清 | 10ml/20ml | -20℃ | 5年 |
细胞成骨诱导分化添加剂A | 1ml/2ml | -20℃ | 1年 |
细胞成骨诱导分化添加剂B | 40ul/80ul | -20℃ | 1年 |
细胞成骨诱导分化添加剂C | 100ul/200ul | -20℃ | 1年 |
赠送产品 | |||
茜素红 | 5ml/10ml | 2-8℃ | 1年 |
明胶水溶液(0.2%) | 5ml/10ml | 2-8℃ | 1年 |
Ø 注意:
1.为保证产品的有效性,请不要反复冻融。
四、实验方法
(1)成骨诱导分化培养基配制
1、本产品为试剂盒型,使用前需将试剂盒内各成分试剂混匀。
2、使用前,请将血清置于4℃解冻,直至血清完全溶解;待血清完全溶解后,将所有添加物置于室温溶解。待试剂完全溶解后,轻轻摇晃使试剂混合均匀。(注:为了保证微量试剂的 使用效果,请将低于 200μL 的试剂管进行短暂离心,使试剂能全部收集至管底。)
3、按上述成分表,将充分溶解混匀的 FBS、青链霉素、β-甘油磷酸钠、抗坏血酸和地塞米松加入到诱导基础培养基中;混合均匀后做好标识,培养基即可使用。(β-甘油磷酸钠溶解性较差,必须确保完全溶解后再加入诱导培养基中
注:(1)无菌吸取试剂管中的试剂成分,将枪头伸至培养基液面下方注入,轻微吹打洗涤枪头。再吸取少量培养基洗涤试剂管,尽可能将所有组分完整地加到基础培养基中,保证培养基的效果。
(2)试剂配制应全程在无菌操作台进行。
(2)成骨诱导分化细胞准备(以六孔板为例)
1、间充质干细胞的融合度达到 80~90%时,用0.25%胰酶进行消化,注意干细胞生长密度不宜过大,易成片脱落。
2. 将消化下来的间充质干细胞进行计数,根据计数结果,按 2×104 cells/cm2 的细 胞密度(根据细胞生长速度,使得在 6 孔板接种后第二天的细胞汇合度达到70%~80%即可) 接种在六孔板中,每孔加入 2mL 的间充质干细胞完全培养基(为防止诱导过程因细胞密度过大出现细胞回缩或漂浮,建议铺板前用明胶包被六孔板)。
3. 将均匀接种好的间充质干细胞置于37℃,5% CO2 的培养箱中进行培养。
4. 当细胞融合度达到70%~80%时,小心的将孔内完全培养基吸走,向六孔板中加入 2 mL 间充质干细胞成骨诱导分化培养基。
5. 每隔3天换用新鲜的间充质干细胞成骨诱导分化培养基(使用前需预热至室温以 上)。(注意:成骨诱导过程中,换液时注意不要把液体打到细胞表面,防止细胞层脱落。)
6. 诱导 2~4 周后,视细胞的形态变化及生长情况,根据您的实验需要进行鉴定。
(3)茜素红染色
1. 吸走孔板里的成骨诱导分化完全培养基,用 1×PBS 冲洗 1~2 遍。
2. 加入 4%多聚甲醛溶液(覆盖细胞表面即可),对细胞固定 30分钟。
3. 吸走 4%多聚甲醛溶液,用 1×PBS 冲洗1~2 遍。
4. 以六孔板为例,每孔加入1mL 茜素红染色液,室温染色 30 分钟(染色时间可以根据细胞染色情况延长或缩减)。
5. 吸走茜素红染色液,用 清水沿壁 冲洗 把背景杂质洗干净,即可在显微镜下观察诱导和 染色效果。
注意事项:
1、仅限科研用。
2、培养体系中的一些组分是对人体健康有害的物质,请不要用暴露的皮肤接触培养体系的液体和有培养体系的液体残留的容器内部;这部分有害物质的浓度和危害性都较低,如有接触,立即用自来水冲洗即可。