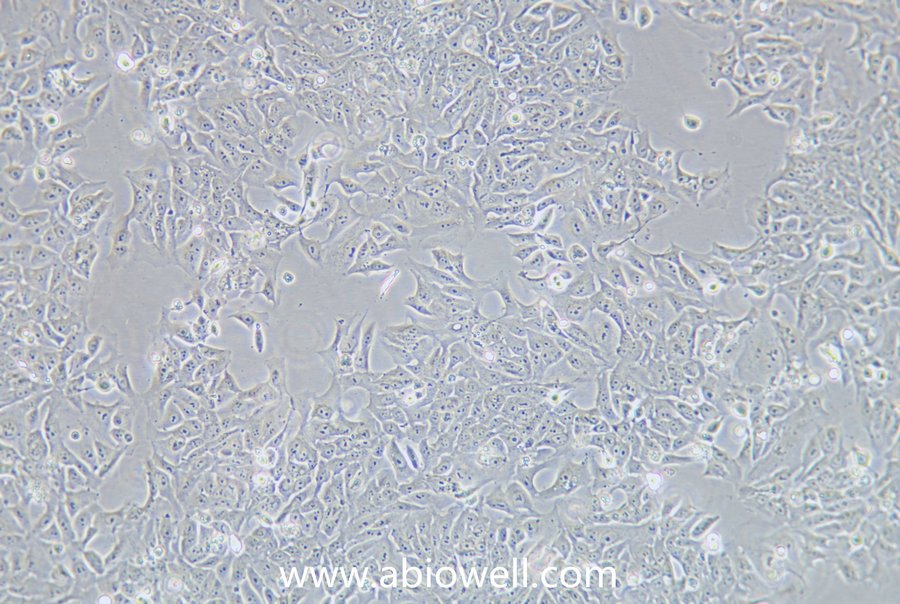
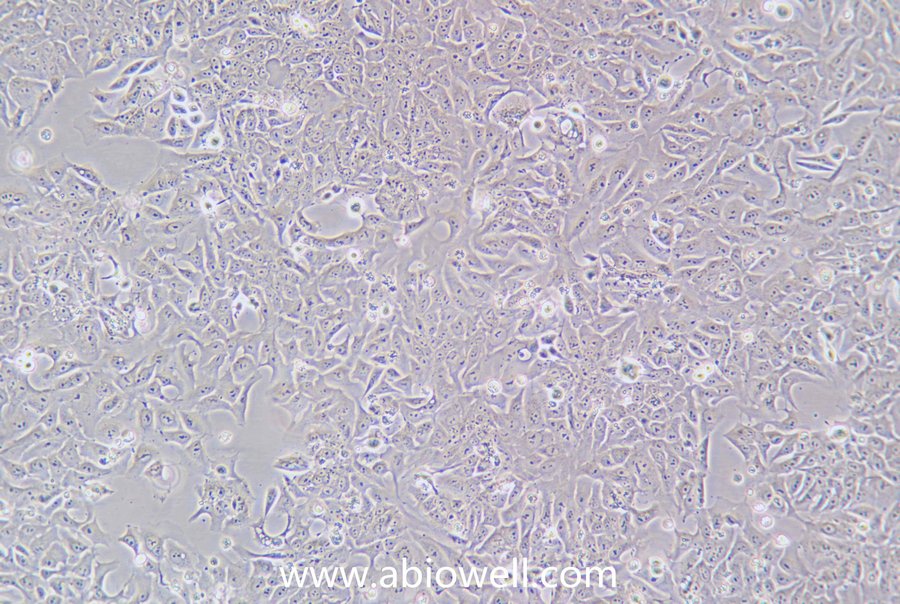
细胞描述:
DLD-1细胞是由D·L·Dexter和其同事于1977-1979年分离的两株结直肠腺癌细胞株中的一株。在ATCC和其它地方进行的DNA指纹鉴定和染色体组型分析表明DLD-1细胞与HCT-15细胞相似,说明这两者是来自同一个人的不同克隆。DLD-1细胞和HCT-15细胞的遗传起源可通过DNA指纹鉴定证实,但染色体组型分析显示它们缺乏染色体标记一致改变或数目上一致改变。DLD-1细胞的CSAp阴性(CSAp-),p53抗原表达呈阳性(p53抗原产生了一个C→T点突变导致241位的Ser→Phe)。DLD-1细胞角蛋白免疫过氧化物酶染色阳性,癌基因c-myc、K-ras、H-ras、N-ras、myb、sis和fos的表达呈阳性,癌基因N-myc的表达未做检测。DLD-1细胞表达肿瘤特异性核基质蛋白CC-2、CC-3、CC-4、CC-5和CC-6。1979年提交到ATCC的DLD-1细胞代数不明且污染了支原体,其后经过12周多种抗生素联合培养处理,处理之后每周用Hoechst染色和标准培养法检测。其后连续11个月不加抗生素培养,DLD-1细胞所有的检测呈阴性。
细胞特性:
1) 来源:人,结直肠腺癌上皮细胞
2) 形态:上皮细胞样,贴壁生长
3) 规格:1×106cells
4) 培养条件:RPMI-1640+10%优质胎牛血清+1%双抗 (推荐货号AW-MC002)
空气,95%;二氧化碳,5%
37℃
细胞接收后的处理:
1) 收到细胞后,活细胞首先观察培养瓶是否完好,培养液是否漏液,培养基是否浑浊;冻存细胞是否干冰已挥发完,冻存管盖是否脱落,破碎,若有这类情况,请务必拍照记录,并于收货24h内与我们联系。
2) 细胞处理:
复苏的细胞:如果是T-25培养瓶活细胞,收到后请用75%的酒精对培养瓶表面进行消毒处理,然后转入培养箱中静置2~3h后再进行后续处理。
备注:运输用的培养基不宜再次用来培养细胞,请按照说明书新配置完全培养基来培养细胞。
冻存细胞:如果是干冰运输的冻存细胞,收到后请立即转入液氮存储或者短暂(24h)放置-80度冰箱保存,或者直接进行细胞复苏。
细胞复苏、传代及冻存流程参考:
1、 细胞复苏
1) 配制完全培养基:基础培养基+胎牛血清+双抗(特殊培养基特殊配置);
2) 细胞复苏:取5ml完全培养基于15ml离心管中,37℃水浴锅预热,从液氮管(或者-80度冰箱)中快速取出冻存的细胞,放入37℃水浴锅中,摇晃使快速化冻(1min左右),然后将化冻的细胞和预热的培养基,移入超净工作台中,化冻的细胞加入到含预热培养基的15ml离心管中,1000rpm离心5min;
3) 吸弃上清,得到细胞沉淀,用2ml完全培养基轻轻重悬细胞,加入到T25培养瓶中,做好标记,放入37℃,5%CO2饱和适度培养箱中培养(培养皿复苏效果更好);
4) 24h后,观察细胞贴壁情况(未贴壁的即为死细胞--针对贴壁细胞),吸弃旧培养基,加入新鲜的预热(室温或37℃)的完全培养基,继续培养。
2、 细胞传代
1) 待细胞生长到80%-90%汇合度时,吸弃旧的培养基,加入1ml无菌PBS润洗一次,以去除残余的培养基及血清(血清含有胰酶的抑制因子),然后加入1ml 0.25%胰酶,37℃培养箱中消化(1~2min左右,不同细胞消化时间不同),取出细胞,镜下观察细胞至细胞皱缩变圆;
2) 加入1ml完全培养基(含FBS)终止消化,轻轻拍打,使细胞脱落下来成单个细胞悬液,收集细胞于15ml无菌离心管中,1000rpm,离心5min;
3) 收集细胞沉淀,完全培养基重悬,一分为二(可根据细胞生长速度调整比例),分别加入到2个新的培养瓶中,做好标记,放入培养箱中培养。
3、细胞冻存
1) 按照细胞传代方法,在超净工作台内消化收集细胞沉淀,取少量细胞用于计数;
2) 用预冷的1ml冻存液(90%完全培养基+10%DMSO)或者无血清细胞冻存液重悬细胞,加入到1.2ml冻存管中,密度为1*106个/ml。
3) 放入程序冻存盒,-80℃过夜后,转入液氮长期保存。